فواید اسید فسفریک چیست؟ فواید اسید فسفریک بسیار زیاد بوده و در زندگی روزمره از آن استفاده می کنیم و چگونه تولید می شود در این مقاله کامل به شما عزیزان توضیحات فواید اسید فسفریک و مراحل تولید را قدم به قدم توضیح داده و کاربرد های آن را کامل به شما گفته ایم پس تا آخر این مقاله با ما همراه باشید. همچنین شما عزیزان می توانید برای تهیه و خرید اسید فسفریک با بالاترین و مرغوب ترین کیفیت و مناسب ترین قیمت به صفحه فروش اسید فسفریک مراجعه نمایید.
اسید فسفریک چیست ؟
اسید فسفریک، همچنین به عنوان اسید فسفریک (V) یا اسید اورتوفسفریک شناخته می شود، یک اسید رایج است. بنابراین شکل خام اسید آنتیس از سنگ فسفات استخراج می شود، در حالی که شکل خالص فسفر سفید به صورت صنعتی تولید می شود. اسید فسفریک خالص به طور کلی یک جامد کریستالی است و غلظت کمی دارد. به طور کلی، این مایع بی رنگ، بی بو، غیر فرار و شربتی است.
اسید فسفریک نیز یک اسید معدنی است . فرمول H3PO4 است که دارای یک اتم فسفر، چهار اتم اکسیژن و سه اتم بی آب است.
اسید فسفریک یک اسید اکسی فسفر با فرمول شیمیایی H3PO4 است، از یک اسید معدنی تشکیل شده است که در آن سه پروتون اسیدی به یک یون فسفات متصل شده است (PO 4 3- ). اگرچه اسید قوی محسوب نمی شود، اما استفاده نادرست از آن می تواند خطراتی برای سلامتی ایجاد کند.
می توان آن را در دو حالت یافت: به صورت یک جامد به شکل بلورهای قطور متعامد یا به صورت مایع کریستالی با ظاهر شربتی. رایج ترین نمایش تجاری آن دارای غلظت 85 درصد وزنی و چگالی 1.685 گرم بر سانتی متر مکعب است . این تراکم از دست تمرکز حاصل می شود.
سه گروه OH مسئول اهدای هیدروژن های اسیدی هستند. به دلیل وجود آنها در ترکیب خود، می تواند نمک های زیادی را با هیدروکسیدهای مختلف تشکیل دهد.
در مورد هیدروکسید سدیم، آن می تواند سه تشکیل دهد: فسفات مونوبازیک سدیم (NaH 2 PO 4 )، سدیم دو بازیک فسفات (Na 2 HPO 4 ) و فسفات سدیم تری بازیک ( Na 3 PO 4 ).
با این حال، بسته به اینکه کدام پایه برای فرمولاسیون آن استفاده می شود، یا اینکه کدام کاتیون بسیار نزدیک به آن است، می تواند نمک های دیگر فسفات را تشکیل دهد. از جمله آنها می توان به فسفات کلسیم (Ca) 3 (PO 4 ) 2 ، لیتیوم فسفات (Li 3 PO 4 ) ، فسفات آهن (FePO 4 ) و غیره اشاره کرد. هر یون فسفات درجه پروتوناسیون خاص خود را دارد.
از سوی دیگر، اسید فسفریک می تواند کاتیون ها را به شکل Fe 2+ ، Cu 2+ ، Ca 2+ و Mg 2+ «جلو» کند. در دماهای بالا می تواند به خودی خود با از دست دادن یک مولکول H 2 یا تشکیل دایمرها، تریمرها و پلیمرهای اسید فسفریک واکنش نشان دهد.
این نوع واکنش این ترکیب را قادر می سازد تا تعداد زیادی ساختار با اسکلت فسفر و اکسیژن ایجاد کند، که از آنها می توان طیف وسیعی از نمک های شناخته شده مانند پلی فسفات ها را نیز به دست آورد.
در ارتباط با کشف آن، رابرت بویل در سال 1694 با حل کردن P 2 O 5 (پنتوکسید فسفر) در آب سنتز کرد. این یکی از اسیدهای معدنی با کاربرد بیشتر است که مهمترین آن عملکرد آن به عنوان کود است. سه ماده غذایی اصلی گیاه همراه با فسفر، پتاسیم و نیتروژن وجود دارد.

ترکیب شیمیایی
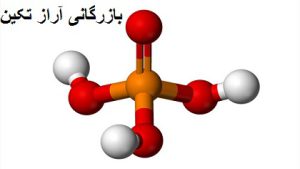
اسید فسفریک دارای یک پیوند P=O و سه P-OH است، که در آن دومی حامل هیدروژنهای اسیدی هستند که در یک محیط تفکیک آزاد میشوند. با اتم فسفر در مرکز، اکسیژن ها نوعی چهار وجهی مولکولی را تشکیل می دهند.
به این ترتیب، اسید فسفریک را می توان به عنوان یک چهار وجهی در نظر گرفت. از این دیدگاه، چهار وجهی (در واحد H 3 PO 4 ) نامیده می شود که با پیوندهای هیدروژنی با یکدیگر برهمکنش می کنند. یعنی گوشه آنها نزدیک است.
این فعل و انفعالات بین مولکولی به اسید فسفریک اجازه می دهد تا به دو جامد متبلور شود: بی آب و همی هیدرات (H 3 PO 4 1/2 H 2 O ) هر دو با سیستم های کریستالی مونوکلینیک . شکل بی آب آن را می توان با این فرمول نیز توصیف کرد: 3H 2 OP 2 O 5 ، معادل پنتوکسید فسفر سه هیدراته.
چهار وجهی حتی می تواند به صورت کووالانسی پیوند بخورد، اما این امر مستلزم حذف یک مولکول آب از یکی از واحدهای آنها با کم آبی است. این زمانی اتفاق می افتد که H 3 PO 4 در معرض حرارت قرار می گیرد و در نتیجه تشکیل اسید پلی فسفریک (PA) را ایجاد می کند.
اسید دی فسفریک (H 4 P 2 O 7 )
ساده ترین PA ها اسید دی فسفریک (H 4 P 2 O 7 ) است که به نام اسید پیروفسفریک نیز شناخته می شود. معادله شیمیایی برای تشکیل آن به شرح زیر است:
2H 3 PO 4 <=> H 4 P 2 O 7 + H 2 O
تعادل به مقدار آب و دما بستگی دارد.

اسید پلی فسفریک
در صورت ادامه گرمایش، کم آبی می تواند با اسید پیروفسفریک ادامه یابد. چرا؟ زیرا در هر انتهای مولکول خود یک گروه OH دارد که می تواند به عنوان یک مولکول آب خاتمه یابد، بنابراین رشد بعدی اسکلت POPOP را افزایش می دهد.
نمونه هایی از این اسیدها اسیدهای تری پلی فسفریک و تتراپلی فسفریک هستند. می توان دید که چگونه اسکلت پاپ در نوعی زنجیره که توسط چهار وجهی تشکیل شده است، پخش می شود.
این ترکیبات را می توان با فرمول HO (PO 2 OH) x H نشان داد، که در آن HO انتهای چپی است که می تواند آبگیری شود. PO 2 OH با اسکلت فسفر P = O و OH پیوند دارد. و x واحدها یا مولکولهای اسید فسفریک مورد نیاز برای بدست آوردن زنجیره مذکور هستند.
هنگامی که این ترکیبات به طور کامل با یک پایه خنثی می شوند، به اصطلاح پلی فسفات ها تولید می شوند. بسته به اینکه آنها را احاطه کرده اند، چندین نوع نمک پلی فسفات را تشکیل می دهند.
از طرف دیگر، اگر نها ا الکل ROH واکنش دهند، دروژن ای اسکلتی نها ا ایگزین لکیل R- ایگزین می ود. نابراین، استرهای سفات (یا لی سفات) ولید می وند: Ro (PO 2 ا) X A.
با این حال، اسید فسفریک معمولاً به عنوان اسید اورتوفسفریک نیز شناخته می شود. چرا؟ زیرا کلمه «اورتو» یونانی است و به معنای «درست» است. شکل “درست” یا “هیدراته تر” این چه خواهد بود؟
هنگامی که انیدرید فسفریک با آب اضافی هیدراته می شود (P 4 O 10 ، “کلاهک” فسفر) تصویر بالا H 3 PO 4 (3H 2 OP 2 O 5 ) تشکیل می شود. بنابراین، پیشوند ارتو به آن دسته از اسیدهایی که با آب فراوان تشکیل می شوند، اختصاص داده می شود.
نخ
پیشوند pyro به تمام ترکیبات تولید شده پس از اعمال گرما اشاره دارد، زیرا اسید دی فسفریک از آبگیری حرارتی اسید فسفریک تولید می شود. بنابراین اسید پیروفسفریک (2H 2 OP 2 O 5 ) نامیده می شود.
هدف
پیشوند متا که یک کلمه یونانی نیز هست به معنای «بعد» است. به موادی اضافه می شود که فرمول آنها یک مولکول، در این مورد، آب را حذف کرده است:
H 3 PO 4 => HPO 3 + H 2 O
توجه داشته باشید که این بار با افزودن دو واحد فسفریک اسید دی فسفریک تشکیل نمی شود، بلکه اسید متافسفریک (که هیچ مدرکی دال بر وجود آن ندارد) به دست می آید.
همچنین مهم است که توجه داشته باشید که این اسید را می توان به عنوان H 2 OP 2 O 5 توصیف کرد (شبیه به همیدرات، ضرب HPO در 3 2). پیشوند متا از PA کاملاً حلقوی پیروی می کند، زیرا اگر اسید تری فسفریک کم آب شود، اما واحد دیگری H 3 PO 4 اضافه نکند تا به اسید تترا فسفریک تبدیل شود، باید یک حلقه تشکیل دهد.
و این مورد در مورد سایر اسیدهای پلی متافسفریک است، اگرچه IUPAC توصیه می کند که آنها را ترکیبات حلقوی PAهای مربوطه نامید.
ویژگی اسید فسفریک
فرمول مولکولی
h 3 po 4
وزن مولکولی
97994 گرم در مول
ظاهر فیزیکی
در شکل جامد خود کریستال های ارتدوکس، رطوبت سنجی و شفاف را ارائه می دهد. در شکل مایع، کریستالی از ظاهر یک شربت چسبناک است.
از نظر تجاری در محلول آبی با غلظت 85 درصد وزنی به دست می آید. همه این ارائه ها فاقد بو هستند.
نقطه جوش و ذوب
158 درجه سانتیگراد (316 درجه فارنهایت تا 760 میلی متر جیوه).
108 فارنهایت (42.2 درجه سانتیگراد).
حلالیت در آب
548 گرم / 100 گرم در H 2 یا 20º C؛ 369.4 گرم در 100 میلی لیتر در 0.5 درجه سانتیگراد. 446 گرم / 100 متر تا 14.95 درجه سانتیگراد.

تراکم
1892 گرم بر سانتی متر 3 (جامد)؛ 1841 گرم بر سانتی متر مکعب ( محلول 100%)؛ 1685 گرم بر سانتی متر 3 (85٪ محلول)؛ 1334 گرم بر سانتی متر مکعب محلول 50 درصد در دمای 25 درجه سانتی گراد).
چگالی بخار
3،4 نسبت به هوا (هوا = 1).
احتراق خودکار
قابل اشتعال نیست.
ویسکوزیته
3.86 mPoise (20 محلول 40٪ در C).
ترشی
pH: 1.5 (محلول 0.1N در آب)
pKa: pKa1 = 2.148; pKa2 = 7,198 و pKa3 = 12,319. در نتیجه، هیدروژن به اضافه اسید آن اولین است.
پوسیدگی
هنگامی که گرم می شود، اکسید فسفر آزاد می کند. اگر دما به 213 درجه سانتیگراد یا بیشتر افزایش یابد به اسید پیروفسفریک تبدیل می شود (H 4 P 2 O 7 ).
خورندگی
خورنده به فلزات آهنی و آلومینیوم. در واکنش با این فلزات گاز سوخت هیدروژن تولید می شود.
بسپارش
با ترکیبات آزو، اپوکسیدها و ترکیبات پلیمریزاسیون پلیمریزه می شود.
کاربرد های اسید فسفریک
نمک های فسفات و مصارف رایج
-اسید فسفریک به عنوان پایه ای برای انبساط فسفات ها عمل می کند که به عنوان کود استفاده می شود زیرا فسفر یک ماده غذایی اصلی برای گیاهان است.
– در مسمومیت با سرب و سایر شرایطی که به مقادیر قابل توجهی فسفات نیاز دارند و اسیدوز خفیف ایجاد می کنند استفاده می شود.
-برای کنترل pH راسو و مجاری ادراری برای جلوگیری از تشکیل سنگ کلیه استفاده می شود.
اسید فسفریک نمک های Na 2 HPO 4 و NaH 2 PO 4 تولید می کند که یک سیستم بافر برای pH با pKa 6.8 تشکیل می دهد.
این سیستم تنظیمی pH در انسان وجود دارد و در تنظیم pH داخل سلولی و همچنین در مدیریت غلظت هیدروژن در لولههای دیستال و جمعکننده نفرون اهمیت دارد.
برای حذف لایه کپک زده اکسید آهن که روی این فلز می نشیند استفاده می شود. اسید فسفریک فسفات آهن را تشکیل می دهد که به راحتی از سطح فلز جدا می شود. همچنین در پولیش الکتریکی آلومینیوم استفاده می شود و یک ماده اتصال دهنده برای محصولات نسوز مانند آلومینا و منیزیم است.
اسید فسفریک صنعتی
اسید فسفریک به عنوان یک عامل کاتالیزوری در ساخت نایلون و بنزین در نظر گرفته شده است. این ماده به عنوان یک عامل آب زدایی در حکاکی لیتوگرافی، در ساخت رنگ برای استفاده در صنعت نساجی، در فرآیند انعقاد لاتکس در صنعت لاستیک و در خالص سازی پراکسید هیدروژن استفاده می شود.
این اسید به عنوان یک افزودنی در نوشابه ها استفاده می شود و در نتیجه به طعم آن کمک می کند. شکر در فرآیند تصفیه حل می شود. همچنین به عنوان یک سیستم بافر در تهیه ژامبون، ژلاتین و آنتی بیوتیک ها عمل می کند.
در توسعه مواد شوینده، در کاتالیز اسیدی تولید استیلن نقش دارد.
از آن به عنوان اسیدولانت در صنعت دامداری و خوراک متعادل برای حیوانات خانگی استفاده می شود. صنعت داروسازی از آن در ساخت داروهای ضد استفراغ استفاده می کند. همچنین در مخلوط ها برای ساخت آسفالت برای هموارسازی زمین و ترمیم ترک ها استفاده می شود.
-اسید فسفریک به عنوان یک کاتالیزور در واکنش هیدراتاسیون آلکان ها برای تولید الکل ها، در درجه اول اتانول، عمل می کند. علاوه بر این، در تعیین کربن آلی در خاک استفاده می شود.
دندان شناسی
توسط دندانپزشکان برای تمیز کردن و حالت دادن به سطح دندان ها قبل از قرار دادن تکیه گاه های دندانی استفاده می شود. همچنین در سفید کردن دندان ها و از بین بردن پلاک های دندانی استفاده می شود. علاوه بر این در ساخت چسب های پروتزهای دندانی استفاده می شود.
محصول زیبایی
اسید فسفریک برای تنظیم pH در تهیه محصولات آرایشی و بهداشتی و مراقبت از پوست استفاده می شود. به عنوان یک عامل اکسید کننده شیمیایی برای تولید کربن فعال استفاده می شود.
تشکیل اسید فسفریک
اسید فسفریک از سنگ های فسفات نوع آپاتیت با هضم با اسید سولفوریک غلیظ تهیه می شود:
Ca 3 (PO 4 ) 2 + 3 H 2 SW 4 + 6 H 2 O => 2 H 3 PO 4 + 3 (CaSO 4 .2H 2 O)
اسید فسفریک بهدستآمده در این واکنش از خلوص پایینی برخوردار است، بنابراین فرآیند خالصسازی را طی میکند که شامل روشهای رسوب، استخراج با حلال، تبلور و تبادل یونی است.
-اسید فسفریک را می توان با حل کردن پنتوکسید فسفر در آب جوش تولید کرد.
همچنین می توان آن را با حرارت دادن فسفر با مخلوطی از هوا و بخار آب به دست آورد:
p 4 (l) + 5 o 2 (g) => p 4 o 10 (s)
P 4 O 10 (s) + H 2 O (g) => 4 H 3 PO 4 (L)
خطرات اسید فسفریک
-چون فشار بخار آن در دمای اتاق کم است، بعید است که بخار آن استنشاق شود، مگر اینکه اسید پاشیده شود. اگر چنین است، علائم استنشاق عبارتند از: سرفه، گلودرد، تنگی نفس و تنگی نفس.
-در ادبیات موردی از ملوانی ذکر شده است که برای مدت طولانی در معرض بخار اسید فسفریک بوده است. او با ضعف عمومی، سرفه خشک، درد قفسه سینه و مشکلات تنفسی مواجه بود. یک سال پس از قرار گرفتن در معرض، اختلال عملکرد راه هوایی واکنشی مشاهده شد.
– تماس پوست با اسید فسفریک می تواند باعث قرمزی، درد، تاول و سوزش پوست شود.
مصرف اسید اعث سوزش دهان و لو، سوزش رون سینه، درد م، استفراغ، وک و افتادگی می ود.
استفاده از اسید فسفریک
اسید ارتوفسفریک یک ماده شیمیایی مهم با کاربردهای گسترده در محصولات صنعتی، کشاورزی و روزمره است. به هر حال، در اینجا به برخی از کاربردهای محبوب فسفریک اسید خواهیم پرداخت.
– زدودن زنگ
– در زمینه مواد غذایی و آشامیدنی.
– مراقبت شخصی
– برای کشاورزی
– داروها
کاربردهای دیگر
اسید فسفریک برای از بین بردن زنگ زدگی استفاده می شود.
در بین اسیدهای مختلف، ایزوفان اسید فسفریک برای زدودن زنگ فلزاتی مانند فولاد استفاده می شود. هنگامی که از این اسید استفاده می شود، با زنگ زدگی رسوب می کند و اکسید آهن معمولی قهوه ای مایل به قرمز (فریک اکسید) را به یک ترکیب سیاه رنگ تبدیل می کند که اکنون فسفات آهن نامیده می شود. این فسفات آهن سیاه به راحتی حذف می شود.
اسید فسفریک در غذا استفاده می شود.
اسید فسفریک اغلب به عنوان یک افزودنی غذایی استفاده می شود. این اسید اسیدیته مواد غذایی مانند مربا، غلات، گوشت های فرآوری شده، پنیرها و غیره را کنترل می کند. به عنوان یک افزودنی غذایی در صنعت نوشیدنی استفاده می شود.
در صنعت نوشابه سازی از اسید فسفریک به عنوان عامل ترش کردن استفاده می شود. این به جلوگیری از تشکیل قارچ و باکتری کمک می کند. همچنین به این نوشیدنی ها طعم می بخشد. با این حال، در مورد مزایای سلامتی این اسید بحث و جدل وجود دارد.
اسید فسفریک مورد استفاده در مراقبت شخصی
اسید فسفریک در فرمولاسیون تم انواع محصولات مراقبت شخصی، از جمله محصولات پاک کننده، محصولات حمام، عطر، محصولات مراقبت از مو، رنگ ها، محصولات ناخن، لوازم آرایشی و سایر محصولات مراقبت از پوست ضروری است.
این محصولات شامل محصولات پاک کننده، محصولات حمام، عطر، محصولات مراقبت از مو، رنگ، محصولات ناخن، لوازم آرایشی و محصولات مراقبت از پوست است. علاوه بر این، از اسید فسفریک نیز برای کنترل کاربرد این محصولات استفاده می شود.
کاربردهای اسید فسفریک کشاورزی
طبق گزارشات، حدود 80 درصد از اسید فسفریک در تولید کودها استفاده می شود. اسید فسفریک به عنوان افزودنی و طعم دهنده در خوراک دام و طیور استفاده می شود.
اسید فسفریک در کاربردهای دارویی
این اسید عمدتاً به عنوان یک واسطه در داروسازی استفاده می شود. یکی از کاربردهای اصلی اسید فسفریک، دندانپزشکی است. به عنوان محلول اچینگ استفاده می شود و اغلب برای تمیز کردن دندان استفاده می شود. از دیگر کاربردهای اسید فسفریک می توان به مواد سفید کننده دندان یا دهان شویه ها اشاره کرد. اسید فسفریک نیز معمولا به عنوان یک عامل ضد تهوع استفاده می شود.
کاربردهای دیگر اسید فسفریک
چند کاربرد دیگر برای این اسید وجود دارد. اسید فسفریک به عنوان یک الکترولیت در سلول های سوختی یا هیدروژن-اکسیژنراتورها استفاده می شود. از اسید فسفریک برای ساخت مواد شوینده مصنوعی و تصفیه آب و فلزات نیز استفاده می شود.
همچنین در صنعت ساختمان سازی برای از بین بردن رسوبات معدنی، لکه های سیمانی و لکه های آب سخت استفاده می شود. به عنوان یک اکسید کننده شیمیایی برای تولید محصولات کربن فعال استفاده می شود.
سوالاتی در مورد اسید فسفریک
1. نام مستعار فسفریک اسید چیست؟
جواب: اسید اورتوفسفریک.
2. فرمول شیمیایی اسید فسفریک را بنویسید.
پاسخ: H3PO4.
3. وزن مولکولی، نقطه جوش و نقطه ذوب اسید فسفریک چقدر است؟
پاسخ: وزن مولکولی = 97.994 گرم در مول، نقطه جوش = 158 درجه اول وزن، نقطه ذوب = 42.35 وزن
4. اسید اورتوفسفریک اسید قوی است یا اسید ضعیف؟ چرا؟
تجزیه و تحلیل: اسید ضعیف به دلیل نقص در آب.
5. فهرست دو نوع اسید فسفریک که به طور گسترده مورد استفاده قرار می گیرند.
پاسخ: از اسید فسفریک برای ناباروری و اسیدی شدن مواد غذایی بسیار استفاده می شود.
خرید اسید فسفریک
شما عزیزان می توانید برای خرید اسید فسفریک صنعتی خوراکی و ایرانی و چینی با بالاترین و مرغوب ترین کیفیت و ارسال به تمام سراسر کسور و با ارائه فاکتور رسمی و غیر رسمی با کارشناسان مجموعه آراز تکین تماس حاصل فرمایید . و همچنین برای دیدن نمونه محصولات بیشتر این شرکت مانند اسید سیتریک و اسید اسکوربیک کلیک نمایید .
09120795991